Phản ứng Cl2 rời khỏi HCl (Khí clo tính năng với nước tạo nên trở thành axit clohidric) là 1 quy trình chất hóa học cần thiết và thịnh hành vô cuộc sống thường ngày hằng ngày. Phản ứng này còn có phần mềm thoáng rộng vô ngành công nghiệp, phát triển hóa hóa học và vô quy trình xử lý nước. Hiểu rõ ràng về phản xạ Cl2 rời khỏi HCl hùn tất cả chúng ta hiểu sâu sắc rộng lớn về đặc thù chất hóa học của những hóa học và vai trò của bọn chúng vô cuộc sống hằng ngày. Cùng thăm dò hiểu nhé.
Lý thuyết về Cl2 rời khỏi Hcl
Phương trình phản xạ Clo tính năng với nước
Cl2+ H2O ⇄ HCl + HClO
Bạn đang xem: Cl2 ra HCl | Phương trình hóa học Cl2 + H2O ⇄ HCl + HClO
Điều khiếu nại phản xạ xảy ra
Nhiệt phỏng thường
Tiến hành phản xạ Clo tính năng với nước
Khi tan nội địa, một trong những phần khí clo tính năng với nước đưa đến lếu láo thích hợp axit clohidric và axit hipoclorơ
Trong phản xạ bên trên, clo vừa vặn là hóa học lão hóa, vừa vặn là hóa học khử vì như thế một phân vẹn toàn tử Cl bị lão hóa trở thành Cl+1, một vẹn toàn tửu Cl bị khử trở thành Cl-1. Phản ứng bên trên là phản xạ thuận nghịch ngợm vì thế HClO là hóa học lão hóa mạnh, rất có thể lão hóa HCl trở thành Cl2và H2O. Cũng vì thế HClO là hóa học lão hóa mạnh nên nước Clo đem tính tẩy color.
Nội dung không ngừng mở rộng về Clo
Khí clo lỏng là gì?
Clo là nhân tố phi kim nằm trong group Halogen, đem kí hiệu chất hóa học là Cl. Nó nằm trong chu kì 3 của bảng tuần trả, đem ái lực năng lượng điện tử tối đa và có tính âm năng lượng điện xếp hạng thứ 3 vô toàn bộ những nhân tố.
Clo tồn bên trên ở hai dạng này là dạng lỏng và dạng khí. Tại dạng khí clo tồn bên trên ở dạng phân tử bao gồm 2 vẹn toàn tử clo links cùng nhau.

Khí clo hóa lỏng là gì?
Tính hóa học lý hóa của khí Clo hóa lỏng
Tính hóa học vật lý
- Clo ở tình trạng khí, làm nên màu vàng lục và mùi hương vô nằm trong hắc ở vô ĐK thông thường.
- Clo nằm trong group hóa độc hại hại
- Khi ở dạng phân tử, nó đem lượng là 71, nên nặng trĩu rất là nhiều đối với bầu không khí.
- Khi tan vừa vặn cần nội địa sẽ tạo nên trở thành nước clo làm nên màu vàng nhạt nhẽo và tan nhiều trong những dung môi cơ học.

Những đặc thù vật lí của clo
Tính hóa học hóa học
- Khí Clo lỏng là 1 phi kim nên đem kỹ năng lão hóa vô nằm trong mạnh.
- Khi tính năng với sắt kẽm kim loại, bọn chúng sẽ tạo nên rời khỏi muối hạt halogenua. điều đặc biệt, clo rất có thể tính năng đa số với toàn cỗ sắt kẽm kim loại, nước ngoài trừ Au và Pt:
2Fe +3Cl2 → 2FeCl3
- Tác dụng với Hidro bọn chúng sẽ tạo nên rời khỏi một thích hợp hóa học khí (Nếu tỉ trọng số mol H2 và Cl2 là 1:1 → lếu láo thích hợp nổ):
H2 + Cl2 → 2HCl
- Tác dụng với nước sẽ tạo nên rời khỏi HCl và HClO, trên đây được gọi là phản xạ nhì chiều:
H2O + Cl2 → HCl + HClO
- Tác dụng với những thích hợp hóa học đem tính khử. Tính Hóa chất của clo cũng có thể có nhiều điểm tương đương với đặc thù chất hóa học của flo và đặc thù chất hóa học của brom. Bởi đó cũng là những hóa học halogen sinh hoạt mạnh:
2FeCl2 + 2NaBr → 2NaCl + Br2
Xem thêm: Sách giáo khoa Hóa học 10 (Cánh Diều) - THI247.com
- Tác dụng với hỗn hợp NaOH muốn tạo trở thành hỗn hợp nước Javen:
Cl2 + 2NaOH → NaCl + NaClO + H2O
Điều chế khí clo lỏng như vậy nào?
Điều chế vô chống thí nghiệm
- Khí clo lỏng được pha chế bằng phương pháp mang lại axit clohidric quánh tính năng với hóa học lão hóa mạnh như mangan đioxit rắn (MnO2) hoặc kali pemanganat rắn (KMnO4)… Chú ý, MnO2 rất cần phải đun rét, với KMnO4 rất có thể đun hoặc ko.
- Khí clo chiếm được thông thường bị láo nháo tạp hóa học là khí hiđro clorua và khá nước, nhằm vô hiệu tạp hóa học, cần thiết dẫn khí clo theo lần lượt qua chuyện những bình cọ khí chứa chấp hỗn hợp NaCl (để lưu giữ khí HCl) và chứa chấp H2SO4 quánh để lưu lại khá nước.
- Các phương trình pha chế như sau:
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 6H2O
Điều chế clo lỏng vô công nghiệp
- Khí Clo vô công nghiệp được pha chế vì chưng cách thức năng lượng điện phân rét chảy muối hạt Natri clorua:
2NaCl → 2Na + Cl2
- Ngoài rời khỏi, người tớ cũng rất có thể dùng cách thức năng lượng điện phân hỗn hợp muối hạt đem màng ngăn như sau:
2NaCl + 2H2O → H2 + 2NaOH + Cl2
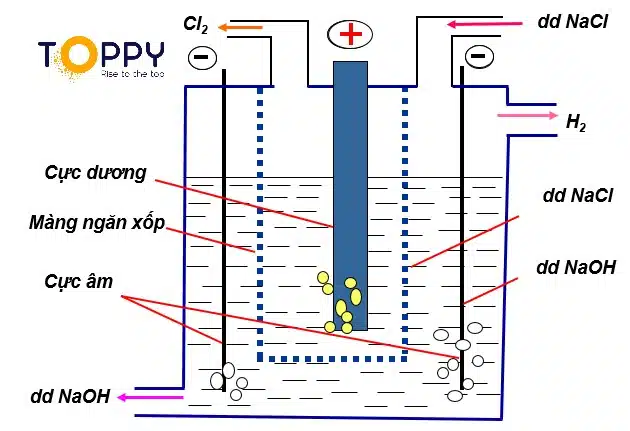
Phương pháp pha chế khí Clo
Những tính năng tuyệt hảo của khí clo
Khí clo là 1 thành phầm được phần mềm vô nằm trong thoáng rộng vô cuộc sống thường ngày và phát triển như sau:
- Ứng dụng vô pha chế vật liệu nhựa PVC cũng như các hóa học mềm hoặc cao su đặc.
- Có tính năng tiệt trùng. Chủ yếu ớt sử dụng khí Clo là thịnh hành nhất. Khi sử dụng vô xử lý nước, bên dưới môi trường thiên nhiên áp suất cao và thực hiện giá thành, nó được fake hóa ở dạng lỏng.
- Sử dụng khí Clo ở dạng axít hipoclorơ HClO sẽ giúp đỡ tiệt trùng vô hồ nước bơi lội, khối hệ thống cấp cho nước, xử lý nước thải…
- Nó còn được sử dụng vô quy trình phát triển giấy tờ, dung dịch nhuộm, dung dịch trừ sâu sắc, sơn… và nhiều dụng cụ dùng hằng ngày không giống.
- Là vật liệu cần thiết sẽ giúp đỡ phát triển nhiều thích hợp hóa học cơ học và vô sinh.

Những tính năng tuyệt hảo của khí clo
Khí clo, clo lỏng đem ô nhiễm hoặc không?
- Khí clo là 1 khí vô nằm trong ô nhiễm mang lại sức mạnh trái đất, tạo nên tổn hại vĩnh viễn, đặc trưng rộng lớn là rất có thể tạo nên tử vong.
- Ảnh hưởng trọn của tỷ lệ 250ppm mang lại một phần hai tiếng rất có thể tạo nên tử vong cho tất cả những người lớn
- Khi hít cần khí clo rất có thể tạo nên kích ứng cao, khi xúc tiếp rất có thể thực hiện rộp domain authority và đôi mắt.
- Nếu phải chịu lâu nhiều năm của khí Clo, tiếp tục khiến cho trái đất trở thành già nua trước tuổi hạc, tạo nên những yếu tố nguy nan về phế truất cai quản, sự làm mòn của răng, những bệnh dịch tương quan cho tới phổi như lao…
- Đối với phụ nữ giới mang bầu dùng nước chứa chấp clo đem nguy cơ tiềm ẩn tạo nên sảy bầu, bị biến dạng.
Câu căn vặn áp dụng liên quan
Câu 1. Trong phản xạ Cl2 + H2O ⇄ HCl + HClO. Vai vô của clo là
- hóa học khử.
- hóa học lão hóa, hóa học khử.
- hóa học lão hóa.
- ko là hóa học lão hóa, hóa học khử.
Câu 2. Khi dẫn khí clo vô nước xẩy ra hiện nay tượng
- hoá học
- vật lí và hoá học
- vật lí
- ko xẩy ra hiện tượng kỳ lạ vật lí và hóa học
Câu 3. Hợp hóa học nào là tại đây phản xạ được với nước Clo
- NaCl
- CaSO4
- Cu(NO3)2
- KOH
Câu 4. Nước clo đem tính tẩy color vì
- khi dẫn khí clo vô nước ko xẩy ra phản xạ hoá học
- clo tính năng với nước tạo thành axit HCl đem tính tẩy màu
- clo hấp phụ được màu
- clo tính năng nước tạo thành axit HClO đem tính tẩy màu
Xem đáp án
————————————-
Xem thêm: Công dân là gì? Các quyền cơ bản của công dân Việt Nam
Trên trên đây, Toppy vẫn cung ứng cho mình phát âm tư liệu về phản xạ chất hóa học Cl2 + H2O ⇄ HCl + HClO. Tuy nhiên, nhằm đạt thành quả cao hơn nữa vô học hành, Toppy ham muốn reviews tăng những tư liệu hữu ích không giống, nằm trong tìm hiểu thêm sau đây nhé.
Xem thêm:
- Tính Hóa chất của Clo lớp 9 – Toppy
- AgCl rời khỏi Cl2 | Phương trình phản xạ chất hóa học AgCl → Cl2 + Ag
- mno2 hcl | Phương trình MnO2 + HCl → MnCl2 + Cl2 + H2O
- KMnO4 rời khỏi Cl2 | KMnO4 + HCl → KCl + MnCl2 + Cl2 + H2O