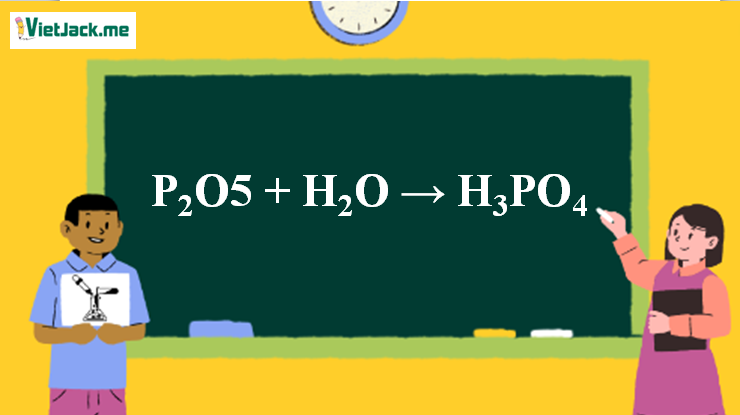P2O5 + H2O → H3PO4 là phản xạ hóa thích hợp. Bài ghi chép này hỗ trợ không hề thiếu vấn đề về phương trình chất hóa học đã và đang được cân đối, ĐK những hóa học nhập cuộc phản xạ, hiện tượng lạ (nếu có), ... Mời chúng ta đón xem:
Phản ứng P2O5 + H2O → H3PO4
Bạn đang xem: P2O5 + H2O → H3PO4 | P2O5 ra H3PO4
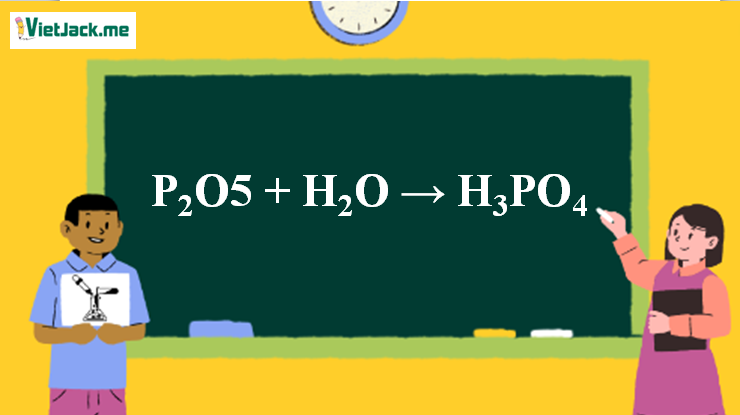
1. Phương trình phản xạ P2O5 ứng dụng H2O
P2O5 + 3H2O → 2H3PO4
2. Điều khiếu nại phản xạ P2O5 ứng dụng với nước
Không có
3. Cách tiến hành phản xạ P2O5 ứng dụng với nước
Cho P2O5 ứng dụng với nước.
4. Hiện tượng nhận ra phản xạ P2O5 ứng dụng với nước
Chất rắn white color Điphotpho pentaoxit (P2O5) tan dần dần. Dung dịch axit H3PO4 thực hiện thay đổi màu sắc giấy tờ quỳ tím trở thành đỏ gay.
5. tin tức không ngừng mở rộng về P2O5
5.1. Tính hóa học vật lý cơ P2O5
Là hóa học sương Trắng, ko mùi hương, háo nước và dễ dàng chảy rữa thông thường dùng để làm thực hiện thô những hóa học.
5.2. Tính hóa học hoá học tập P2O5
Tác dụng với hỗn hợp kiềm, tùy từng tỉ trọng rất có thể tạo nên trở thành những muối hạt không giống nhau:
P2O5 + 2NaOH + H2O → 2NaH2PO4
P2O5 + 4NaOH → 2Na2HPO4 + H2O
P2O5 + 6NaOH→ 2Na3PO4 + 3H2O
Tác dụng với nước
P2O5+ 3H2O → 2H3PO4(axit photphoric)
P2O5 + H2O → 2HPO3 (axit metaphotphoric)
5.3. Điều chế P2O5
4P + 5O2→ 2P2O5
5.4. Ứng dụng P2O5
Công dụng chủ yếu của Tripoly P2O5 là được dùng thực hiện hóa học mút hút độ ẩm mang lại hóa học lỏng và khí. Bên cạnh đó nó còn được sử dụng nhập quy trình tổ hợp cơ học.
Trong tiến độ phát triển andehyt thì này lại được phối hợp cùng theo với axit cacboxylic.
Một phần mềm không giống của Tripoly là làm công việc phân bón nhập phát triển nông lâm nghiệp như phân lân photphat.
6. Tính hóa chất của H2O
6.1. Nước ứng dụng với kim loại
Ở ĐK thông thường, nước rất có thể phản xạ với những sắt kẽm kim loại mạnh như Li, Ca, Na, K, Ba,… sẽ tạo trở thành hỗn hợp Bazo và khí Hidro.
H2O + Kim loại → Bazơ + H2↑
2M + 2nH2O → 2M(OH)n + nH2↑
2Na + 2H2O → 2NaOH + H2
2K + 2H2O → 2KOH + H2
Ca + 2H2O → Ca(OH)2 + H2
Ba + 2H2O → Ba(OH)2 + H2
Đặc biệt, một trong những sắt kẽm kim loại tầm như Mg, Zn, Al, Fe,…phản ứng được với tương đối nước ở nhiệt độ phỏng cao dẫn đến oxit sắt kẽm kim loại và hidro. Ngoài ra, sắt kẽm kim loại Mg tan rất rất lờ lững nội địa rét.
6.2. Nước ứng dụng với oxit bazo
Nước ứng dụng với một trong những oxit bazo như Na2O, CaO , K2O,… tạo nên trở thành hỗn hợp bazo ứng. Dung dịch bazo thực hiện mang lại quỳ tím hóa xanh rớt.
H2O + Oxit bazơ → Bazơ
Na2O + H2O → 2NaOH
Li2O + H2O→ 2LiOH
K2O + H2O→ 2KOH
CaO + H2O → Ca(OH)2
6.3. Nước ứng dụng với oxit axit
Nước ứng dụng với oxit axit tạo nên trở thành axit ứng. Dung dịch axit thực hiện quỳ tím hóa đỏ gay.
H2O + Oxit axit → Axit
CO2 + H2O → H2CO3
SO2 + H2O → H2SO3
P2O5 + 3H2O → 2H3PO4
SO3 + H2O → H2SO4
N2O5 + H2O → 2HNO3
7. Bài tập luyện vận dụng
Câu 1. Cho a gam P2O5 ứng dụng với 507 ml hỗn hợp NaOH 2M, sau thời điểm những phản xạ xẩy ra trọn vẹn nhận được hỗn hợp A. Cô cạn hỗn hợp A nhận được 6a gam hóa học rắn. Giá trị của a là:
A. 21,3
B. 8,52
C.12,78
D. 17,04
Lời giải:
Đáp án: D
Giải thích:
Xét tình huống 1:
P2O5và NaOH pứ một vừa hai phải đầy đủ tạo nên muối:
nH2O = nNaOH = 1,014 mol.
P2O5+ H2O → 2H3PO4
a/142 → 2a/142 mol
Có thể xẩy ra những phương trình chất hóa học sau:
H3PO4 + NaOH → NaH2PO4+ H2O (3)
H3PO4 + 2NaOH → Na2HPO4+ 2H2O (4)
H3PO4 + 3NaOH → Na3PO4+ 3H2O (5)
Áp dụng bảo toàn lượng tớ có:
mH3PO4 + mNaOH= mrắn + mH2O
(2a/142).98 + 1,014.40 = 6a + 1,014.18
→ a = 13,772 gam (loại).
Trường thích hợp 2: Chất rắn gồm: NaOH dư; Na3PO4
P2O5 + 6NaOH→ 2Na3PO4 + 3H2O
a/142 1,014 2a/142 3a/142
Áp dụng bảo toàn khối lượng:
mP2O5 + mNaOHbđ = mrắn + mH2O
a + 0.507.2.40 = 3a + 18.6a/142 => a = 17,04 gam.
Câu 2. Đốt trọn vẹn m gam photpho nhập oxi dư, rồi mang lại thành phầm ứng dụng với hỗn hợp NaOH dư, nhận được 41,0 gam muối hạt. Giá trị của m là
A. 7,75
B. 31,0
C. 15,5
D. 46,5
Lời giải:
Đáp án: A
Giải thích:
Phương trình phản xạ xảy ra
4P + 5O2 → 2P2O5
P2O5+ 6NaOH dư → 2Na3PO4 + 3H2O
=> nNa3PO4 = 41/164 = 0,25 (mol)
Bảo toàn thành phần P.. tớ có
nP = nNa3PO4 = 0,25 (mol)
=> mP = 0,25.31 = 7,75 (gam)
Câu 3. Cho 7,1 gam P2O5 nhập 100 ml hỗn hợp NaOH 1,5M nhận được hỗn hợp X. Cô cạn hỗn hợp X được lếu láo thích hợp bao gồm những hóa học là
A. NaH2PO4 và H3PO4.
B. NaH2PO4và Na2HPO4.
C. NaH2PO4 và Na3PO4.
D. Na3PO4 và Na2HPO4.
Lời giải:
Đáp án: B
Giải thích:
Ta có
nP2O5 = 0,05 mol;
nNaOH= 0,15 mol = 3nP2O5
=> Phản ứng dẫn đến 2 muối hạt là NaH2PO4 và Na2HPO4
Phương trình phản ứng
P2O5 + 2NaOH + H2O → 2NaH2PO4
P2O5 + 4NaOH → 2Na2HPO4 + H2O
Câu 4. Trộn 3 hỗn hợp HCl 0,3M; H2SO4 0,2M; và H3PO4 0,1M với những thể tích đều bằng nhau nhận được hỗn hợp A. Để hòa hợp 300 ml hỗn hợp A cần thiết một vừa hai phải đầy đủ V ml hỗn hợp B bao gồm NaOH 0,2M và Ba(OH)20,1M. Giá trị của V là
A. 250.
B. 200.
C. 500.
D. 550.
Lời giải:
Đáp án: B
Giải thích:
Thể tích từng axit là 100ml
nH+ = nHCl + 2nH2SO4+ 3nH3PO4= 0,1.0,3+ 2.0,2.0,1+ 3.0,1.0,1 = 0,1 mol
nOH-= (V.0,1+2.0,2.V)/1000 mol
H+ + OH- → H2O
Theo phương trình: nH+= nOH-
nên 0,1= (V.0,1 + 2.0,2.V)/1000 suy đi ra V= 200 ml
Câu 5. Cho 300 ml hỗn hợp KOH 1M ứng dụng với 400 ml hỗn hợp H3PO4 0,5M. Sau phản xạ, nhập hỗn hợp chứa chấp những muối
A. KH2PO4 và K2HPO4.
B. KH2PO4 và K3PO4.
C. K2HPO4 và K3PO4.
D. KH2PO4, K2HPO4và K3PO4
Lời giải:
Đáp án: A
Giải thích:
Ta có: nKOH = 0,3 (mol); nH3PO4 = 0,2 (mol)
Ta thấy: 1 < nKOH/nH3PO4= 0,3/0,2 = 1,5 < 2 → Tạo muối hạt KH2PO4 và K2HPO4
Câu 6. Cho 22 gam NaOH nhập hỗn hợp chứa chấp 19,6 gam H3PO4. Sau Khi phản xạ xẩy ra trọn vẹn, rước cô cạn hỗn hợp. Khối lượng từng muối hạt khan nhận được là
A. 50 gam Na3PO4.
B. 7,1 gam Na2HPO4 và 24,6 gam Na3PO4.
C. 15 gam NaH2PO4.
D. 24,6 gam Na2HPO4 và 49,2 gam Na3PO4.
Lời giải:
Đáp án: B
Giải thích:
nNaOH = 22/40 = 0,55 mol;
nH3PO4 = 19,6/98 = 0,2 mol
Ta có: 2< nNaOH/nH3PO4 = 0,55/0,2 = 2,75 < 3 phản xạ sinh đi ra 2 muối hạt là Na2HPO4 (x mol) và Na3PO4 (y mol)
Phương trình hóa học
Xem thêm: Soạn bài Vắt cổ chày ra nước, May không đi giày | Ngắn nhất Soạn văn 8 Chân trời sáng tạo.
2NaOH + H3PO4 → Na2HPO4 + 2H2O
2x ← x ← x
3NaOH + H3PO4→ Na3PO4 + 3H2O
3y ← nó ← y
nNaOH = 2x + 3y = 0,55 (1)
nH3PO4 = x + nó = 0,2 (2)
Từ (1) và (2) → x = 0,05; nó = 0,15
mNa2HPO4= 0,05.142 = 7,1 gam
mNa3PO4= 0,15.164 = 24,6 gam
→ mmuối = 7,1 + 24,6 = 31,7 gam
Câu 7. Nhận xét này tại đây đích thị ?
A. Thành phần chủ yếu của quặng apatit là 3Ca3(PO4)2, CaF2.
B. Trong công nghiệp photpho được pha trộn kể từ Ca3P2, SiO2 và C.
C. Tại ĐK thông thường photpho đỏ gay ứng dụng với O2 dẫn đến thành phầm P2O5.
D. Các muối hạt Ca3(PO4)2 và CaHPO4 đều tan nội địa.
Lời giải:
Đáp án: A
Giải thích:
A. Thành phần chủ yếu của quặng apatit là 3Ca3(PO4)2, CaF2.
Câu 8. Khi sập KOH cho tới dư nhập dd H3PO4, sau phản xạ xẩy ra trọn vẹn nhận được muối
A. K3PO4 và K2HPO4
B. KH2PO4
C. K3PO4
D. K3PO4 và KH2PO4
Lời giải:
Đáp án: C
Câu 9. Câu vấn đáp này sau đây ko đúng vào lúc nói tới axit photphoric?
A. Axit photphoric là axit có tính mạnh trung bình
B. Axit photphoric là axit thân phụ nấc.
C. Axit photphoric với tính lão hóa cực mạnh.
D. Axit photphoric thực hiện quỳ tím gửi red color.
Lời giải:
Đáp án: C
Giải thích:
Axit phophoric là axit 3 nấc, có tính mạnh tầm, rất có thể thực hiện quỳ tím hóa đỏ gay và với tính lão hóa trung bình
Câu 10. Chỉ đi ra những oxit bazo: P2O5, CaO, CuO, BaO, Na2O, P2O3
A. P2O5, CaO, CuO
B. CaO, CuO, BaO, Na2O
C. BaO, Na2O, P2O3
D. P2O5, CaO, P2O3
Lời giải:
Đáp án: B
Câu 11: Chỉ đi ra oxit axit: P2O5, CaO, CuO, BaO, SO2, CO2
A. P2O5, CaO, CuO, BaO
B. BaO, SO2, CO2
C. CaO, CuO, BaO
D. SO2, CO2 , P2O5
Lời giải:
Đáp án: D
Câu 12: Chọn đáp án đúng
A. CO- cacbon (II) oxit
B. CuO- đồng (II) oxit
C. FeO- Fe (III) oxit
D. CaO- can xi trioxit
Lời giải:
Đáp án: B
Câu 13: Axit ứng của CO2
A. H2SO4
B. H3PO4
C. H2CO3
D. HCl
Lời giải:
Đáp án: C
Câu 14: Bazo ứng của MgO
A. Mg(OH)2
B. MgCl2
C. MgSO4
D. Mg(OH)3
Lời giải:
Đáp án: A
Câu 15: Tên gọi của P2O5
A. Điphotpho trioxit
B. Photpho oxit
C. Điphotpho oxit
D. Điphotpho pentaoxit
Lời giải:
Đáp án: D
Câu 16. Phản ứng thân thuộc cặp hóa học này tại đây ko xảy ra?
A. Dung dịch bari hiđroxit và hỗn hợp axit clohiđric
B. Dung dịch đồng (II) sunfat và hỗn hợp natri hiđroxit
C. Dung dịch natri cacbonat và hỗn hợp kali clorua
D. Dung dịch bari clorua và hỗn hợp natri sunfat
Lời giải:
Đáp án: C
Giải thích:
Ba(OH)2 + 2HCl → BaCl2 + H2O
CuSO4 + NaOH → Cu(OH)2 + Na2SO4
BaCl2 + Na2SO4→ BaSO4 + NaCl
Câu 17. Phản ứng thân thuộc cặp hóa học này tại đây dẫn đến thành phầm với hóa học khí?
A. Dung dịch natri hiđroxit và hỗn hợp axit sunfuric
B. Dung dịch natri cacbonat và hỗn hợp bari hiđroxit
C. Dung dịch bari clorua và hỗn hợp natri sunfat
D. Dung dịch natri sunfit và hỗn hợp axit clohiđric
Lời giải:
Đáp án: D
Giải thích:
Phương trình chất hóa học.
Na2SO3 + 2HCl → 2NaCl + H2O + SO2
Câu 18. Hấp thụ trọn vẹn 11,2 lít khí CO2 (đktc) bởi vì một hỗn hợp chứa chấp trăng tròn g NaOH. Muối được tạo nên trở thành là:
A. Na2CO3.
B. NaHCO3.
C. Hỗn thích hợp Na2CO3 và NaHCO3.
D. Na(HCO3)2.
Lời giải:
Đáp án: B
Giải thích:
nCO2= 11,2/22,4 = 0,5 mol;
nNaOH = 20/ 40 = 0,5 mol
T = nNaOH/nCO2 = 0,5/0,5 = 1 mol
Sau phản xạ nhận được muối hạt NaHCO3
Câu 19. Hoà tan 6,2 g natri oxit nhập 193,8 g nước thì được hỗn hợp A. Nồng phỏng xác suất của hỗn hợp A là:
A. 4%.
B. 6%.
C. 4,5%
D. 10%
Lời giải:
Đáp án: A
Giải thích:
nNa2O = mNa2O/MNa2O =6,22/(23 + 16) = 0,1 (mol)
Phương trình hóa học:
Na2O + H2O → 2NaOH
0,1 0,1 0,2
Theo phương trình hóa học:: nNaOH = 2nNa2O = 2.0,1 = 0,2 (mol)
⟹ mNaOH = nNaOH. MNaOH = 0,2.40 = 8 (g)
Khối lượng hỗn hợp sau là: mdd sau = mNa2O + mH2O = 6,2 + 193,8 = 200 (g)
Dung dịch A nhận được là hỗn hợp NaOH
Nồng phỏng xác suất C%NaOH = mNaOH/mddsau.100% = 8/200.100% = 4 %
Câu trăng tròn. Dãy những hóa học ứng dụng với diêm sinh đioxit là:
A. Na2O, CO2, NaOH, Ca(OH)2
B. CaO, K2O, KOH, Ca(OH)2
C. HCl, Na2O, Fe2O3, Fe(OH)3
D. Na2O, CuO, SO3, CO2
Lời giải:
Đáp án: B
Giải thích:
CaO + SO2 → CaSO3
K2O + SO2 → K2SO3
KOH + SO2 → K2SO3 + H2O
Ca(OH)2 + SO2 → CaSO3 + H2O
Câu 21. Để nhận ra 3 khí ko màu: SO2, O2, H2 đựng nhập 3 lọ mất mặt nhãn tớ dùng:
A . Giấy quỳ tím ẩm
B . Giấy quỳ tím độ ẩm và sử dụng que đóm cháy dở còn tàn đỏ
C . Than hồng bên trên que đóm
D . Dẫn những khí nhập nước vôi trong
Xem thêm: Tìm tập hợp các số nguyên là ước của 6 - thu phương
Lời giải:
Đáp án: B
Giải thích: